الورم الحبيبي لم الخلايا لانغرهانس العظمي: دليل شامل للمرضى مع الأستاذ الدكتور محمد هطيف
الخلاصة الطبية
الورم الحبيبي لم الخلايا لانغرهانس العظمي (LCH) هو اضطراب نادر يتميز بتكاثر خلايا لانغرهانس غير الطبيعية، ويصيب العظام بشكل شائع. يشمل العلاج التجريف الجراحي، حقن الستيرويدات، العلاج الكيميائي، أو العلاج الموجه، مع التركيز على استعادة وظيفة العظم وتقليل المضاعفات تحت إشراف الأستاذ الدكتور محمد هطيف.
الخلاصة الطبية الشاملة: الورم الحبيبي لم الخلايا لانغرهانس العظمي (LCH) هو اضطراب نادر يتميز بتكاثر خلايا لانغرهانس غير الطبيعية، ويصيب العظام بشكل شائع مسبباً تآكلاً وآفات. يتطلب تشخيصه الدقيق وإدارته الشاملة خبرة متخصصة لضمان أفضل النتائج. يشمل العلاج طيفاً واسعاً من الخيارات، بدءاً من المراقبة النشطة وحقن الستيرويدات الموضعية، وصولاً إلى التدخلات الجراحية كالتجريف أو الاستئصال، وقد يتطلب في بعض الحالات علاجاً كيميائياً أو موجهاً. يركز العلاج على استعادة وظيفة العظم، تقليل الألم، ومنع المضاعفات الخطيرة مثل الكسور المرضية أو العجز العصبي. في صنعاء، يبرز الأستاذ الدكتور محمد هطيف، أستاذ جراحة العظام في جامعة صنعاء بخبرته التي تتجاوز العقدين، كمرجع أساسي في تشخيص وعلاج هذه الحالات المعقدة، مستخدماً أحدث التقنيات الجراحية مثل الجراحة المجهرية وتنظير المفاصل بتقنية 4K، ملتزماً بأعلى معايير النزاهة الطبية لضمان أفضل رعاية للمرضى.

مقدمة عميقة: فهم الورم الحبيبي لم الخلايا لانغرهانس العظمي (LCH)
يُعد الورم الحبيبي لم الخلايا لانغرهانس (Langerhans Cell Histiocytosis - LCH) اضطراباً نادراً ومعقداً، ينبع من خلل في خلايا لانغرهانس، وهي نوع من الخلايا المناعية التي توجد بشكل طبيعي في الجلد والأغشية المخاطية ونخاع العظم. في حالات LCH، تتكاثر هذه الخلايا بشكل غير طبيعي وتتجمع في أنسجة مختلفة من الجسم، مكونة آفات أو أوراماً حبيبية. على الرغم من تصنيفه كنوع من الأورام الالتهابية، إلا أن LCH ليس سرطاناً بالمعنى التقليدي، ولكنه يتشارك معه بعض الخصائص مثل النمو غير المنظم للخلايا والقدرة على الانتشار. تتراوح شدة المرض وطيفه السريري بشكل واسع، من آفات منفردة قد تشفى تلقائياً دون تدخل، إلى مرض عدواني متعدد البؤر يؤثر على أنظمة متعددة في الجسم، وقد يسبب مضاعفات خطيرة ومهددة للحياة.
تُعتبر إصابة العظام، المعروفة بالورم الحبيبي لم الخلايا لانغرهانس العظمي، هي الشكل الأكثر شيوعاً لهذا المرض، حيث تمثل 80-90% من جميع حالات LCH. يمكن أن تتأثر أي عظمة في الجسم، ولكن المواقع الشائعة تشمل الجمجمة (خاصة العظام الجدارية والصدغية)، العظام الطويلة (مثل عظم الفخذ والعضد والظنبوب)، الفقرات (مما قد يؤدي إلى "الفقرة المسطحة")، والحوض. يُظهر المرض توزيعاً عمرياً ثنائي الذروة، حيث يبلغ ذروته في مرحلة الطفولة المبكرة (خاصة بين 1-4 سنوات) وذروة أصغر في مرحلة البلوغ (20-40 سنة). يُقدر معدل الإصابة بحوالي 5-9 حالات لكل مليون طفل سنوياً، مما يجعله مرضاً نادراً يتطلب خبرة متخصصة للتشخيص والعلاج. يُلاحظ أن الذكور يتأثرون بشكل طفيف أكثر من الإناث.
الشاغل الأساسي في طب الأورام العظمية هو الطبيعة المدمرة لهذه الآفات (Osteolytic)، والتي تعمل على تآكل العظم وإضعافه. هذا التآكل يمكن أن يؤدي إلى:
* كسور مرضية: كسور تحدث في عظم ضعيف بسبب المرض نفسه وليس بسبب إصابة قوية، مما يزيد من الألم ويعيق الحركة.
* عدم استقرار العمود الفقري: خاصة عند إصابة الفقرات، مما قد يسبب آلاماً شديدة في الظهر، تشوهات في العمود الفقري (مثل الحداب)، أو في الحالات الشديدة، ضغطاً على الحبل الشوكي.
* عجز عصبي: في حالات نادرة، إذا ضغطت الآفات على الحبل الشوكي أو الأعصاب المحيطة، قد تؤدي إلى ضعف في الأطراف، خدر، أو حتى شلل.
* تشوهات هيكلية وجمالية: خاصة في الجمجمة أو العظام الوجهية، مما قد يؤثر على جودة حياة المريض.
يُعد التشخيص الدقيق والإدارة المناسبة والمتعددة التخصصات أمراً بالغ الأهمية لتحسين النتائج وتقليل الآثار طويلة المدى. في صنعاء، يقدم الأستاذ الدكتور محمد هطيف، استشاري جراحة العظام والعمود الفقري، خبرة لا تقدر بثمن في هذا المجال، حيث يجمع بين المعرفة الأكاديمية العميقة (كأستاذ في جامعة صنعاء) والمهارة الجراحية الفائقة، مع التزامه بالنزاهة الطبية وتقديم الرعاية الأكثر حداثة وفعالية.
التشريح المرضي وتأثير الورم الحبيبي لم الخلايا لانغرهانس على العظام
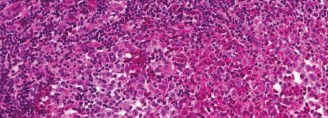
لفهم كيفية تأثير الورم الحبيبي لم الخلايا لانغرهانس العظمي، يجب استعراض كيفية عمل العظام وتأثرها بهذا الاضطراب. العظام هي هياكل ديناميكية تتكون من خلايا عظمية وهيكل معدني معقد يوفر الدعم والحماية. عملية إعادة تشكيل العظام (Bone Remodeling) هي عملية مستمرة يتم فيها إزالة العظم القديم بواسطة خلايا ناقضة للعظم (Osteoclasts) وبناء عظم جديد بواسطة خلايا بانية للعظم (Osteoblasts). في حالات LCH العظمي، تتجمع خلايا لانغرهانس غير الطبيعية، بالإضافة إلى خلايا التهابية أخرى، داخل نسيج العظم. هذا التجمع يؤدي إلى:
- تنشيط الخلايا الناقضة للعظم: تفرز خلايا لانغرهانس وعوامل الالتهاب مواد كيميائية تحفز الخلايا الناقضة للعظم على العمل بشكل مفرط، مما يؤدي إلى تآكل العظم بشكل أسرع من قدرة الخلايا البانية للعظم على إعادة بنائه.
- تكوين الآفات الحالة للعظم (Osteolytic Lesions): نتيجة لتآكل العظم، تتشكل مناطق ضعيفة أو ثقوب داخل العظم، تظهر على الأشعة السينية كآفات شفافة أو "حفر". هذه الآفات هي السمة المميزة لـ LCH العظمي.
- ضعف الهيكل العظمي: يؤدي تآكل العظم إلى إضعاف البنية العظمية، مما يجعلها عرضة للكسور المرضية حتى مع إصابات طفيفة.
المواقع العظمية الأكثر شيوعاً وتأثيراتها:
- الجمجمة: تُعد الجمجمة من أكثر المواقع تأثراً. الآفات هنا يمكن أن تكون مفردة أو متعددة. الأعراض تشمل كتلة محسوسة، ألم موضعي، أو تشوه في شكل الجمجمة. في بعض الحالات النادرة، قد تؤثر الآفات على قاعدة الجمجمة مسببة أعراضاً عصبية أو اضطرابات هرمونية (مثل مرض السكري الكاذب إذا تأثرت الغدة النخامية).
- الفقرات (العمود الفقري): إصابة الفقرات شائعة، خاصة في العمود الفقري الصدري والقطني. يمكن أن تؤدي إلى انهيار الفقرة، مما يعرف بـ "الفقرة المسطحة" (Vertebra Plana)، حيث تفقد الفقرة ارتفاعها وتصبح مسطحة. هذا يمكن أن يسبب آلاماً شديدة في الظهر، تحدباً (Kyphosis)، وفي الحالات المتقدمة، ضغطاً على الحبل الشوكي مما يؤدي إلى ضعف أو شلل في الأطراف.
- العظام الطويلة (الفخذ، العضد، الظنبوب): تظهر الآفات عادة في منطقة الكردوس (Diaphysis) أو المشاش (Metaphysis) من العظم. الأعراض تشمل ألماً موضعياً، تورماً، وحساسية عند اللمس. تزيد هذه الآفات من خطر الكسور المرضية بشكل كبير.
- الحوض: يمكن أن تسبب الآفات الحوضية ألماً في الورك أو الفخذ، وقد تؤثر على المشي والحركة.
- عظام أخرى: يمكن أن تتأثر عظام الفك، الأضلاع، الترقوة، وعظام اليدين والقدمين، مما يسبب ألماً وتورماً موضعياً.
الأسباب والعوامل المؤهبة للورم الحبيبي لم الخلايا لانغرهانس العظمي
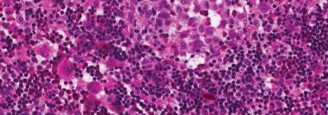
على الرغم من التقدم في فهم LCH، لا يزال السبب الدقيق للمرض غير معروف بالكامل. ومع ذلك، تشير الأبحاث الحديثة إلى أن LCH ليس مجرد اضطراب التهابي، بل هو اضطراب ورمي (Neoplastic) ينشأ من خلايا لانغرهانس التي خضعت لتغيرات جينية.
النظريات والأسباب المحتملة:
-
الطفرات الجينية:
- طفرة BRAF V600E: تُعد هذه الطفرة الجينية هي الأكثر شيوعاً، حيث توجد في حوالي 50-60% من حالات LCH. هذه الطفرة تسبب فرط نشاط في مسار إشارات الخلية (MAPK pathway)، مما يؤدي إلى تكاثر غير منظم لخلايا لانغرهانس. اكتشاف هذه الطفرة فتح الباب أمام العلاجات الموجهة.
- طفرات أخرى: تم تحديد طفرات أخرى في جينات مثل MAP2K1 و ARAF، والتي تؤثر أيضاً على مسار MAPK، في بعض الحالات التي لا تحتوي على طفرة BRAF.
- الوراثة: LCH ليس مرضاً وراثياً بالمعنى التقليدي، أي أنه لا ينتقل مباشرة من الآباء إلى الأبناء. الطفرات الجينية المذكورة هي طفرات جسدية (Somatic Mutations)، تحدث في خلايا معينة بعد الولادة وليست موروثة.
-
الخلل في الجهاز المناعي:
- يُعتقد أن هناك خللاً في تنظيم الجهاز المناعي يلعب دوراً في تطور LCH. تتفاعل خلايا لانغرهانس غير الطبيعية مع خلايا مناعية أخرى (مثل الخلايا التائية والبائية والخلايا البلعمية)، مما يؤدي إلى استجابة التهابية مزمنة تساهم في تدمير الأنسجة.
- قد تكون هناك عوامل محفزة بيئية أو فيروسية تؤدي إلى هذا الخلل المناعي لدى الأفراد المعرضين جينياً، لكن لا يوجد دليل قاطع على ذلك حتى الآن.
-
العوامل البيئية:
- تم اقتراح بعض العوامل البيئية كمحفزات محتملة، مثل التعرض للتدخين السلبي في الطفولة، أو بعض أنواع العدوى الفيروسية، لكن الأدلة على هذه الروابط لا تزال غير حاسمة وتحتاج إلى مزيد من البحث.
عوامل الخطر:
- العمر: كما ذكرنا، يظهر المرض ذروتين عمريتين، في الطفولة المبكرة وفي مرحلة الشباب.
- الجنس: الذكور يتأثرون بشكل طفيف أكثر من الإناث.
- التاريخ العائلي: لا يوجد تاريخ عائلي واضح للمرض في معظم الحالات.
الأهمية السريرية لفهم الأسباب:
إن فهم الطفرات الجينية المحددة في خلايا LCH له أهمية كبيرة في تطوير علاجات موجهة أكثر فعالية وأقل سمية، خاصة في الحالات المقاومة للعلاج التقليدي أو المتعددة الأنظمة.
الأعراض والعلامات السريرية للورم الحبيبي لم الخلايا لانغرهانس العظمي
تعتمد الأعراض السريرية للورم الحبيبي لم الخلايا لانغرهانس العظمي بشكل كبير على موقع الآفة وحجمها، وكذلك على ما إذا كان المرض يؤثر على عضو واحد (Single System Disease) أو عدة أعضاء (Multi-System Disease).
الأعراض الموضعية (خاصة بالآفات العظمية):
- الألم: هو العرض الأكثر شيوعاً. يمكن أن يكون الألم مزمناً، موضعياً، ويزداد سوءاً مع النشاط أو في الليل. في الأطفال، قد يظهر الألم كعرج أو رفض استخدام الطرف المصاب.
- التورم والكتلة المحسوسة: قد يشعر المريض بكتلة صلبة أو تورم في المنطقة المصابة، خاصة في الجمجمة أو العظام الطويلة السطحية.
- الكسور المرضية: في حالات ضعف العظم الشديد، قد يحدث كسر في العظم المصاب حتى مع إصابة طفيفة أو بدون سبب واضح. هذا قد يكون العرض الأول للمرض.
- التشوهات الهيكلية:
- في الجمجمة: قد تسبب الآفات تشوهات في شكل الجمجمة أو نتوءات عظمية.
- في العمود الفقري: انهيار الفقرات (Vertebra Plana) يمكن أن يؤدي إلى آلام حادة في الظهر، تحدب (Kyphosis)، أو اعوجاج في العمود الفقري.
- الأعراض العصبية: نادرة ولكنها خطيرة، تحدث إذا ضغطت الآفة العظمية على الحبل الشوكي أو الأعصاب المحيطة. قد تشمل:
- ضعف أو خدر في الأطراف.
- صعوبة في المشي أو فقدان التوازن.
- فقدان السيطرة على المثانة أو الأمعاء (في حالات ضغط الحبل الشوكي الشديد).
- مشاكل الأسنان والفك: إذا أصاب المرض عظام الفك، قد يؤدي إلى فقدان الأسنان، التهاب اللثة، أو آلام في الفك.
الأعراض الجهازية (إذا كان المرض يؤثر على أعضاء أخرى):
على الرغم من أن تركيزنا هنا على الورم الحبيبي لم الخلايا لانغرهانس العظمي، فمن المهم ملاحظة أن المرض قد يؤثر على أعضاء أخرى، مما يسبب أعراضاً جهازية:
- الحمى: حمى غير مبررة ومستمرة.
- فقدان الوزن: فقدان غير مبرر للوزن.
- الطفح الجلدي: طفح جلدي مزمن، خاصة في فروة الرأس أو منطقة الحفاضات عند الأطفال الصغار.
- تضخم الكبد والطحال والعقد اللمفية: قد تكون هذه الأعراض علامة على مرض متعدد الأنظمة.
- مشاكل في الغدة النخامية: مثل السكري الكاذب (Central Diabetes Insipidus)، والذي يسبب عطشاً شديداً وتبولاً مفرطاً، يحدث إذا تأثرت الغدة النخامية بآفة LCH.
- مشاكل في الرئة: سعال، ضيق في التنفس.
جدول الأعراض الشائعة للورم الحبيبي لم الخلايا لانغرهانس العظمي حسب الموقع
| موقع الآفة العظمية | الأعراض الشائعة | المضاعفات المحتملة |
|---|---|---|
| الجمجمة | ألم موضعي، تورم، كتلة محسوسة، تشوه في شكل الرأس. | مشاكل جمالية، ضغط على الدماغ (نادر)، السكري الكاذب. |
| العمود الفقري | ألم شديد في الظهر، تصلب، تشوه (تحدب، اعوجاج). | انهيار الفقرة (Vertebra Plana)، ضغط الحبل الشوكي، ضعف عصبي. |
| العظام الطويلة | ألم موضعي، تورم، حساسية عند اللمس، عرج. | كسور مرضية، تشوه الطرف، صعوبة في الحركة. |
| الحوض | ألم في الورك أو الفخذ، صعوبة في المشي. | كسور مرضية، قيود في حركة الورك. |
| الفك | ألم في الفك، تورم، فقدان الأسنان، التهاب اللثة. | صعوبة في المضغ والكلام، مشاكل جمالية. |
التشخيص المبكر والدقيق أمر حيوي، وتتطلب هذه الأعراض مراجعة فورية لطبيب متخصص في جراحة العظام، مثل الأستاذ الدكتور محمد هطيف في صنعاء، الذي يمتلك الخبرة اللازمة لتقييم هذه الحالات المعقدة ووضع خطة علاجية فعالة.
التشخيص الدقيق: ركيزة العلاج الفعال
يعتمد التشخيص الدقيق للورم الحبيبي لم الخلايا لانغرهانس العظمي على مجموعة من الفحوصات السريرية والتصويرية والنسيجية. نظراً لندرة المرض وتنوع مظاهره، يتطلب الأمر خبرة متخصصة لتمييزه عن حالات أخرى مشابهة.
1. الفحص السريري والتاريخ المرضي:
يبدأ التشخيص بأخذ تاريخ مرضي مفصل، بما في ذلك الأعراض، مدتها، ومدى تأثيرها على حياة المريض. يقوم الأستاذ الدكتور محمد هطيف بإجراء فحص سريري شامل لتقييم موقع الألم، وجود أي كتل محسوسة، مدى حركة المفاصل، وتقييم أي علامات على ضعف عصبي.
2. الفحوصات التصويرية:
تُعد الفحوصات التصويرية حجر الزاوية في الكشف عن الآفات العظمية وتقييم مدى انتشارها.
* الأشعة السينية (X-ray): غالباً ما تكون هي الفحص الأولي. تظهر الآفات العظمية كآفات حالّة للعظم (Osteolytic lesions) ذات حواف واضحة أو غير منتظمة، وقد تظهر "الفقرة المسطحة" في العمود الفقري.
* التصوير المقطعي المحوسب (CT Scan): يوفر تفاصيل أدق عن بنية العظم، ويساعد في تحديد مدى تآكل العظم، وجود أي كسر، وعلاقة الآفة بالهياكل المحيطة، وهو أمر حاسم للتخطيط الجراحي.
* التصوير بالرنين المغناطيسي (MRI): يُستخدم لتقييم الأنسجة الرخوة المحيطة بالآفة، ومدى امتدادها داخل نخاع العظم، ووجود أي ضغط على الحبل الشوكي أو الأعصاب.
* مسح العظام بالنظائر المشعة (Bone Scintigraphy): يمكن أن يساعد في تحديد وجود آفات متعددة في العظام التي قد لا تكون واضحة في الأشعة السينية التقليدية.
* التصوير المقطعي بالإصدار البوزيتروني (PET Scan): قد يُستخدم في بعض الحالات لتقييم النشاط الأيضي للآفات وتحديد مدى انتشار المرض في الجسم (خاصة في حالات المرض متعدد الأنظمة).
3. الخزعة (Biopsy): التشخيص المؤكد:
التشخيص النهائي لـ LCH يتطلب دائماً الحصول على عينة من النسيج المصاب وفحصها تحت المجهر بواسطة أخصائي علم الأمراض.
* خزعة بالإبرة (Needle Biopsy): يتم أخذ عينة صغيرة باستخدام إبرة رفيعة تحت توجيه الأشعة السينية أو التصوير المقطعي.
* خزعة مفتوحة (Open Biopsy): يتم إجراؤها جراحياً، حيث يتم إزالة جزء أكبر من الأنسجة. غالباً ما يفضل الأستاذ الدكتور محمد هطيف الخزعة المفتوحة في الحالات العظمية التي تتطلب تدخلاً جراحياً، حيث يمكن أخذ عينة كافية للتحليل النسيجي والوراثي.
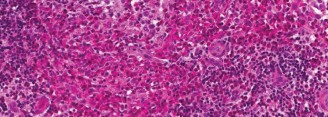
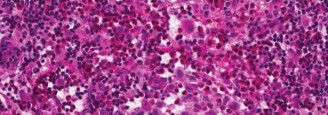
* الفحص النسيجي: يُظهر وجود خلايا لانغرهانس المميزة (التي تحتوي على حبيبات بيربيك - Birbeck granules) بالإضافة إلى خلايا التهابية أخرى.
* الفحص المناعي الكيميائي (Immunohistochemistry): يؤكد التشخيص عن طريق تحديد بروتينات معينة على سطح خلايا لانغرهانس، مثل CD1a و S100.
* الفحص الجيني الجزيئي: يتم إجراء اختبارات للكشف عن طفرات جينية مثل BRAF V600E، والتي تعتبر مهمة لتوجيه العلاج في بعض الحالات.
4. الفحوصات المخبرية:
- تحاليل الدم الروتينية: قد تظهر تعداد دم طبيعياً، أو فقر دم خفيف، أو ارتفاعاً في علامات الالتهاب (مثل ESR و CRP) في بعض الحالات.
- وظائف الكلى والكبد: لتقييم صحة الأعضاء الأخرى.
- فحص البول: في حالات السكري الكاذب، يظهر بول مخفف جداً.
التشخيص الشامل يتطلب نهجاً متعدد التخصصات، حيث يتعاون الأستاذ الدكتور محمد هطيف مع أخصائيي الأشعة، أخصائيي علم الأمراض، وأخصائيي الأورام لضمان الوصول إلى التشخيص الأكثر دقة ووضع خطة علاجية مخصصة لكل مريض.
خيارات العلاج الشاملة للورم الحبيبي لم الخلايا لانغرهانس العظمي
يعتمد علاج الورم الحبيبي لم الخلايا لانغرهانس العظمي على عدة عوامل، بما في ذلك عمر المريض، موقع الآفة وحجمها، ما إذا كانت الآفة مفردة أو متعددة، وما إذا كان المرض يؤثر على أعضاء أخرى. الهدف الأساسي للعلاج هو تخفيف الألم، استعادة وظيفة العظم، منع الكسور المرضية، وتقليل خطر تكرار المرض. يتبع الأستاذ الدكتور محمد هطيف نهجاً علاجياً متكاملاً وشخصياً، مستفيداً من أحدث التطورات الطبية والتقنيات الجراحية.
1. المراقبة النشطة (Observation):
- الاستطباب: في حالات نادرة، خاصة عند الأطفال، قد تشفى الآفات العظمية المنفردة والصغيرة تلقائياً.
- النهج: يتم مراقبة المريض عن كثب من خلال الفحوصات السريرية والأشعة السينية الدورية لتقييم حجم الآفة ونشاطها. يُفضل هذا النهج إذا كانت الآفة غير مؤلمة ولا تسبب ضعفاً هيكلياً كبيراً.
2. العلاج التحفظي (Conservative Treatment):
- الأدوية المضادة للالتهاب غير الستيرويدية (NSAIDs): لتخفيف الألم والالتهاب المرتبط بالآفة.
- حقن الستيرويدات الموضعية: يمكن حقن الكورتيكوستيرويدات مباشرة داخل الآفة العظمية لتقليل الالتهاب وتثبيط نشاط خلايا لانغرهانس. هذا الخيار فعال في بعض الآفات المنفردة والصغيرة، ويقدمه الأستاذ الدكتور محمد هطيف كأحد الخيارات المتاحة قبل اللجوء للجراحة.
3. العلاج الجراحي (Surgical Treatment):
يُعد التدخل الجراحي أحد الركائز الأساسية في علاج الورم الحبيبي لم الخلايا لانغرهانس العظمي، خاصة في الآفات التي تسبب ألماً شديداً، ضعفاً هيكلياً، أو ضغطاً على الهياكل الحيوية. يُعرف الأستاذ الدكتور محمد هطيف بمهارته الجراحية الفائقة وخبرته الواسعة في هذه الإجراءات.
- التجريف (Curettage): هو الإجراء الجراحي الأكثر شيوعاً. يتضمن إزالة الأنسجة المرضية من داخل العظم باستخدام أداة خاصة تسمى "المجرفة".
- الهدف: إزالة خلايا LCH غير الطبيعية، تخفيف الضغط داخل العظم، والحفاظ على أكبر قدر ممكن من العظم السليم.
- دوره: يستخدم الأستاذ الدكتور محمد هطيف التجريف بدقة عالية، وفي بعض الحالات قد يتبعه استخدام عوامل مساعدة مثل الكي الكيميائي (مثل الفينول) أو الكي بالتبريد (Cryoablation) لتقليل خطر تكرار المرض.
- الاستئصال (Excision): في حالات الآفات الصغيرة والمحدودة جيداً، يمكن استئصال الآفة بالكامل مع هامش أمان من العظم السليم.
- الترقيع العظمي (Bone Grafting): بعد التجريف أو الاستئصال، إذا كانت هناك فجوة كبيرة في العظم، قد يقوم الأستاذ الدكتور محمد هطيف بملء الفجوة باستخدام طعم عظمي (Autograft من المريض نفسه أو Allograft من متبرع) أو مواد اصطناعية لتعزيز قوة العظم وتشجيع الشفاء.
- التثبيت الداخلي (Internal Fixation): في حالات الكسور المرضية أو عدم استقرار العمود الفقري، قد يتطلب الأمر تثبيت العظم باستخدام الصفائح والبراغي أو القضبان للمساعدة في شفاء الكسر وتوفير الاستقرار. يستخدم الأستاذ الدكتور محمد هطيف أحدث تقنيات التثبيت لضمان أفضل النتائج.
4. العلاج الكيميائي (Chemotherapy):
- الاستطباب: يُستخدم العلاج الكيميائي في حالات المرض متعدد الأنظمة، أو الآفات العظمية المتعددة، أو الحالات التي لا تستجيب للعلاج الموضعي، أو في المرض الذي يصيب الأعضاء "الخطرة" (مثل الكبد، الطحال، الرئة، الجهاز العصبي المركزي).
- الأدوية الشائعة: الفينبلاستين (Vinblastine) والبريدنيزون (Prednisone) هي الأدوية الأكثر استخداماً.
- النهج: يتم إدارة العلاج الكيميائي بالتعاون مع أخصائيي الأورام، ويشرف الأستاذ الدكتور محمد هطيف على تقييم استجابة الآفات العظمية للعلاج.
5. العلاج الموجه (Targeted Therapy):
- الاستطباب: في حالات LCH التي تحتوي على طفرة BRAF V600E، يمكن استخدام مثبطات BRAF (مثل Vemurafenib أو Dabrafenib) والتي تستهدف هذه الطفرة بشكل خاص.
- الفعالية: أظهرت هذه العلاجات نتائج واعدة في الحالات المقاومة للعلاج التقليدي.
6. العلاج الإشعاعي (Radiation Therapy):
- الاستطباب: يُستخدم العلاج الإشعاعي بشكل محدود في LCH، عادةً لآفات معينة لا يمكن الوصول إليها جراحياً، أو في الحالات التي لا تستجيب للعلاجات الأخرى، أو لتخفيف الألم في الآفات الكبيرة.
- الجرعات: تستخدم جرعات منخفضة نسبياً من الإشعاع.
جدول مقارنة خيارات العلاج الرئيسية للورم الحبيبي لم الخلايا لانغرهانس العظمي
| خيار العلاج | الآلية | الاستطبابات الرئيسية | المزايا | العيوب/المخاطر |
|---|---|---|---|---|
| المراقبة النشطة | متابعة تطور الآفة دون تدخل. | آفات منفردة، صغيرة، غير مؤلمة، شفاء ذاتي محتمل. | تجنب التدخلات الطبية. | خطر النمو أو المضاعفات إذا لم تشفى. |
| حقن الستيرويدات | تقليل الالتهاب وتثبيط الخلايا. | آفات منفردة، صغيرة، يمكن الوصول إليها. | إجراء طفيف التوغل، فعال في بعض الحالات. | قد لا يكون فعالاً لجميع الآفات، خطر تكرار المرض. |
| التجريف الجراحي | إزالة الأنسجة المرضية من داخل العظم. | آفات مؤلمة، كبيرة، تسبب ضعفاً هيكلياً، تشخيص مؤكد |
آلام العظام والمفاصل وتقييد حركتها ليس قدراً محتوماً! التشخيص الدقيق والعلاج المتخصص يمكن أن يعيد لك كامل وظيفتك وحريتك في الحركة. لا تدع الألم يسيطر على حياتك.
للحصول على استشارة دقيقة وخطة علاجية مخصصة لحالتك، تواصل فوراً مع مركز الأستاذ الدكتور محمد هطيف:
الأستاذ الدكتور محمد هطيف - أفضل دكتور عظام في صنعاء، وخبير في جراحات العظام والمفاصل والعمود الفقري.. نلتزم بإعادتك لحياة خالية من الألم وحركة طبيعية.
مواضيع أخرى قد تهمك